آموزش الکترونیک مقدماتی – فصل اول

الکتریسیته
نوعی انرژی است که توسط انرژی های دیگر ایجاد شده و می تواند به سایر انرژی ها تبدیل شود. برای درک انرژی الکتریسیته باید مفاهیمی از ساختمان اتم را بدانیم که در مطالب زیر به آن اشاره کرده ایم.
ساختمان اتم
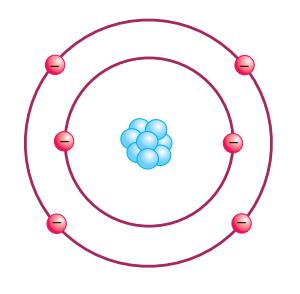
هر اتم از سه نوع ذره تشکیل می شود : الکترون ، پروتون ، نوترون . پروتون ها در مرکز یا هسته ی اتم قرار گرفته اند.
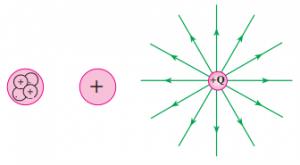
۱- پروتون: بسیار کوچک است و قطر آن۱/۳ قطر الکترون است . پروتون ها در عبور یا انتقال انرژی الکتریکی نقش فعالی ندارند آن ها بار الکتریکی مثبت دارند و بنابر قرارداد ، خطوط نیروی الکتریکی به صورت شعاعی و به طور مستقیم در تمام جهت از پروتون خارج می شوند.
۲- نوترون: نوترون ذره ای است که اگر تجزیه شود ، یک پروتون و یک الکترون حاصل می آید . نوترون از نظر بار الکتریکی خنثی است و بنابراین ، در ماهیت الکتریکی اتم ها چندان مهم تلقی نمی شود .
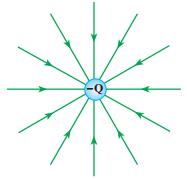
۳- الکترون: الکترون ها را به آسانی می توان حرکت داد . آن ها ذراتی هستند که در انتقال انرژی الکتریکی اثر فعالی دارند . خطوط نیروی وارد شده از هسته به صورت شعاعی و در تمام جهات به الکترون وارد می شود.
نظریه الکترونی
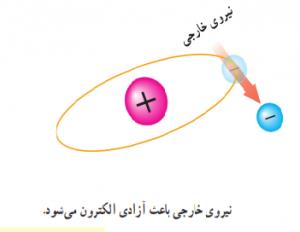
طبق نظریه الکترونی الکتریسیته هنگامی ایجاد می شود که الکترون ها از اتمشان خارج شوند . همانطور می دانیم که الکترون ها با سرعت بسیاری به دور هسته ی اتم در حال چرخش هستند و نیروی گریز از مرکز زیاد آن ها باعث خارج شدن آن ها از مدارشان می شود اما نیروی جاذبه ی مثبت هسته از این عمل جلوگیری می کند .
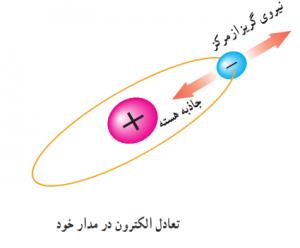
حال اگر یک نیروی خارجی خیلی قوی به اتم داده شود تا به این نیروی گریز از مرکز کمک کند ، الکترون از اتم خود خارج می شود.
لایه ها
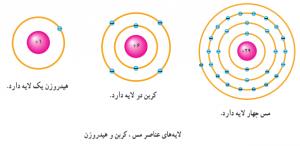
الکترون ها در اتم در لایه های مختلفی به دور هسته در حال گردش می باشند . الکترون های مدارِ نزدیک به هسته به سختی آزاد می شوند ؛ زیرا به نیروی مثبت نگاه دارنده ی خود بسیار نزدیک اند . هرچه الکترون ها از هسته دور تر باشند ، شدت این نیروی مثبت کم تر می شود .
هرچه تعداد الکترون های یک اتم بیش تر باشد ، مدار های بیشتری وجود دارند .
مسیر مداری الکترون ها را لایه (Shell) می گویند .
اتم های تمام عناصر شناخته شده می توانند تا هفت لایه داشته باشند .
ظرفیت لایه ها : ظرفیت هر لایه نشان دهنده ی تعداد الکترونی است که می تواند در خود جای دهد که از رابطه زیر بدست می آید .
ظرفیت لایه = ۲n^2
(n شماره لایه مورد نظر می باشد )
لایه ی خارجی (طبقه والانس): لایه ی خارجی هر اتمی نمی تواند بیش تر از ۸ الکترون داشته باشد . لایه ی خارجی یک اتم لایه ی والانس و الکترون های آن الکترون های والانس نام دارند .
هادی
به ماده ای که الکترون هایش به راحتی می توانند آزاد شوند ، هادی می گویند. اتم های هادی های خوب فقط ۱ یا ۲ الکترون والانس دارد.
علت این موضوع این است که چون انرژی داده شده به اتم بین تمام الکترون های لایه والانس آن تقسیم می شود ، اگر الکترون های لایه والانس کمتر باشد سهم انرژی هر الکترون بیشتر بوده و الکترون راحت تر آزاد می شود .
بهترین هادی ها به ترتیب نقره ، مس و طلا می باشند که هر سه دارای ۱ الکترون والانس می باشند اما علت این که هدایت نقره نسبت به مس و طلا بهتر است این است که در یک مقدار معین از این ۳ ماده نقره اتم های بیشتری دارد ، پس هدایت بهتری نیز دارد .
عایق
عایق ها موادی هستند که آزاد کردن الکترون های مدار آخر آنها بسیار مشکل است .لایه والانس اتم های عایق ، معمولا ۸ الکترون یا دارای ۴ الکترون یا بیشتر هستند.
نیمه هادی
لایه والانس هادی ها کم تراز ۴ الکترون ولایه والانس عایق ها بیشتر از ۴ الکترون دارند. به عناصری که دارای ۴ الکترون والانس دارند ، نیمه هادی می گویند.
امیدواریم تا این لحظه از آموزش ها و مبانی الکترونیک وبسایت استفاده لازم را برده باشید. در فصلهای بعدی به کمیت های الکتریکی ، قطعه شناسی و مفاهیم کلی الکترونیک اشاره خواهد شد.















